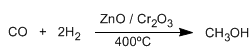
O metanol é un líquido incoloro, o seu punto de ebullición é 65ºC, miscible en auga en todas as proporcións e venenoso (35 ml poden matar unha persoa)
A metade do metanol producido se oxida a metanal (formaldehído), material de partida para a fabricación de resinas e plásticos.
O etanol obtense por fermentación de materia vegetal, obténdose unha concentración máxima de 15% en etanol. Por destilación pódese aumentar esta concentración ata o 98%.
Tamén se pode obter etanol por hidratación do etileno (eteno) que se obtén a partir do petróleo.
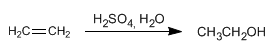
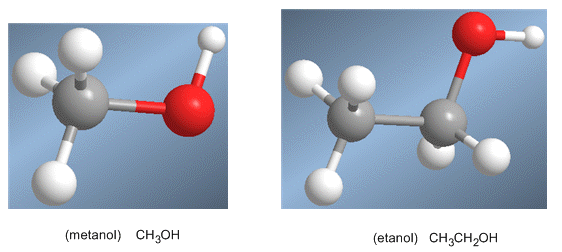
O etanol é un líquido incoloro, miscible en auga en todas proporcións, con punto de ebullición de 78ºC. É fácilmente metabolizado polos nosos organismos, aínda que o seu abuso causa alcoholismo.
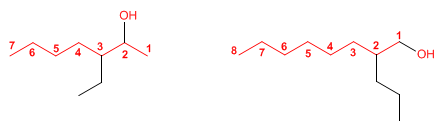
- Regra 1. Elíxese como cadea principal a de maior lonxitude que conteña o grupo -OH.

- Regra 2. Se numera a cadea principal para que o grupo -OH tome o localizador máis baixo. O grupo hidroxilo ten preferencia sobre cadeas carbonadas, halógenos, dobres e triplos enlaces.
- Regra 3. O nome do alcohol constrúese cambiando a terminación -ou do alcano con igual número de carbonos por -ol.
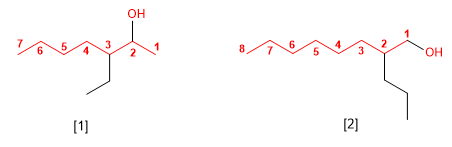
- Regra 4. Cando na molécula hai grupos grupos funcionales de maior prioridad, o alcohol pasa a serun mero sustituyente e chámase hidroxi-. Son prioritarios fronte aos alcohois: acedos carboxílicos, anhídridos, ésteres, haluros de alcanoilo, amidas, nitrilos, aldehídos e cetonas.
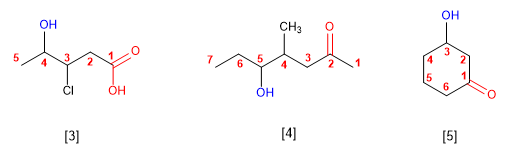
- Regra 5. O grupo -OH é prioritario fronte aos alquenos e alquinos. A numeración outorga o localizador máis baixo ao -OH e o nome da molécula termina en -ol.
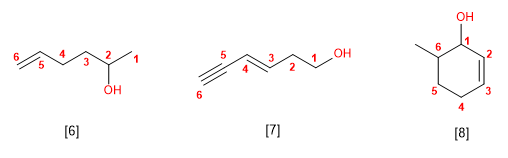
Os alcohois son especies anfóteras (anfipróticas), poden actuar como acedos ou bases. En disolución acuosa establécese un equilibrio entre o alcohol, a auga e as súas bases conxugadas.
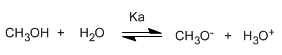
Escribindo a constante do equilibrio (Ka)
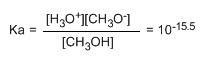
O pequeno valor da constante indícanos que o equilibrio está totalmente desprazado á esquerda. O logaritmo cambiado de signo da constante de equilibrio dános o pKa do metanol, parámetro que indica o grado de acidez dun composto orgánico.
pKa = - log ka = 15.5
O aumento do pKa supón unha disminución da acidez. Asi, o metanol cun pka de 15.5 é ligeramente máis acedo que o etanol con pka de 15.9.
O pKa dos alcohois vese influenciado por algúns factores como son o tamaño da cadea carbonada e os grupos electronegativos
Ao aumentar o tamaño da cadea carbonada o alcohol vólvese menos acedo.
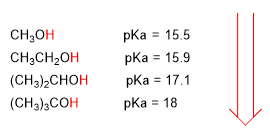
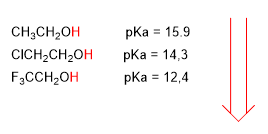
Os grupos electronegativos (halógenos) aumentan a acidez dos alcohois (baixan o pKa)
Alcoholes y fenoles:
No hay comentarios:
Publicar un comentario